本站消息 近日,学校动物医学院江康峰副教授在生物医学领域国际权威期刊《Materials Today Bio》(中科院双一区TOP期刊,影响因子:10.2)上发表题为“Exosomal lncRNA OTUD6B-AS1 as a pathogenic nanocarrier promotes inflammatory macrophage polarization in endometritis via a targetable ceRNA circuit”的研究论文。该研究首次揭示了外泌体作为天然纳米信使,通过传递关键长链非编码RNA驱动子宫内膜炎性损伤的全新机制,为炎症性繁殖障碍疾病的防控开辟了新路径。

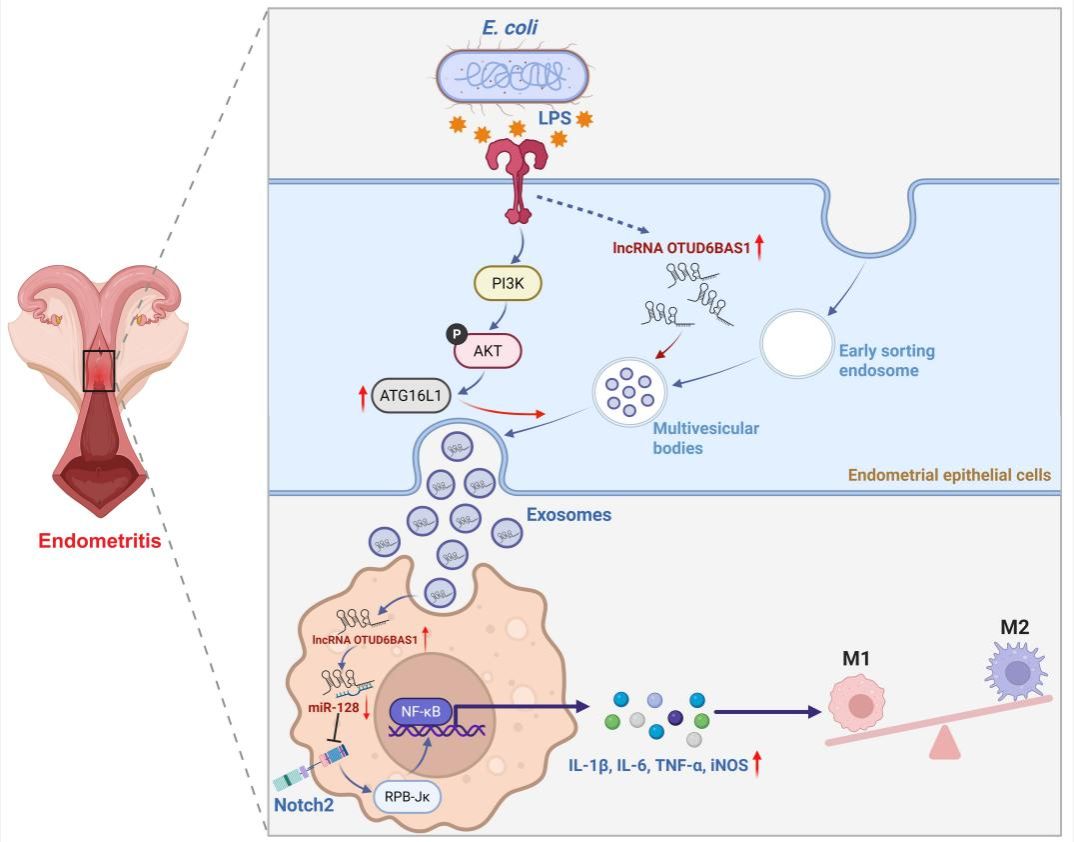
子宫内膜炎是人类和哺乳动物(包括奶牛)中普遍存在的繁殖障碍性疾病,严重影响生殖健康和生产效益。尽管巨噬细胞介导的炎症反应在该病发生发展中起关键作用,但子宫内膜微环境中局部炎症信号如何在细胞间传播扩散的机制尚不明确。本研究以奶牛子宫内膜炎为模型,发现受损的子宫内膜上皮细胞通过AKT/ATG16L1依赖的通路显著增加外泌体的分泌,这些外泌体作为天然的“纳米信使”,将富集的lncRNA OTUD6B-AS1递送至巨噬细胞。lncRNA OTUD6B-AS1通过竞争性内源RNA机制吸附miR-128,解除其对靶基因Notch2的抑制,进而激活NF-κB炎症通路,驱动巨噬细胞向促炎M1表型极化,最终加剧子宫内膜组织损伤。该信号调控轴在临床样本中也进一步得到验证。此外,通过基因敲低lncRNA OTUD6B-AS1或药物干预miR-128/Notch2节点,可有效阻断外泌体的促炎效应。这一发现不仅深化了子宫内膜炎分子机制的理解,更提出了将外泌体作为可调控的天然纳米载体,通过干预其携带的lncRNA cargo实现精准抗炎治疗的新思路,为子宫内膜炎等繁殖障碍疾病的干预提供了重要的理论基础和潜在靶点。
学校动物医学院为本论文唯一完成单位。江康峰副教授与尹革芬教授为共同通讯作者,杨静副教授、硕士研究生陈雅静及博士研究生王奎为共同第一作者。李小兵教授、硕士研究生密丽芳及2022级动物医学专业本科生陈雨姗参与了部分研究工作。该研究得到了云南省重要畜禽疫病防控关键技术创新团队(项目编号:202405AS350004)及国家自然科学基金(项目编号:32202885、32560879)的资助。
(未经允许 严禁转载)
